US-Forschungsteam gibt Patienten durch CRISPR die Sehkraft zurück
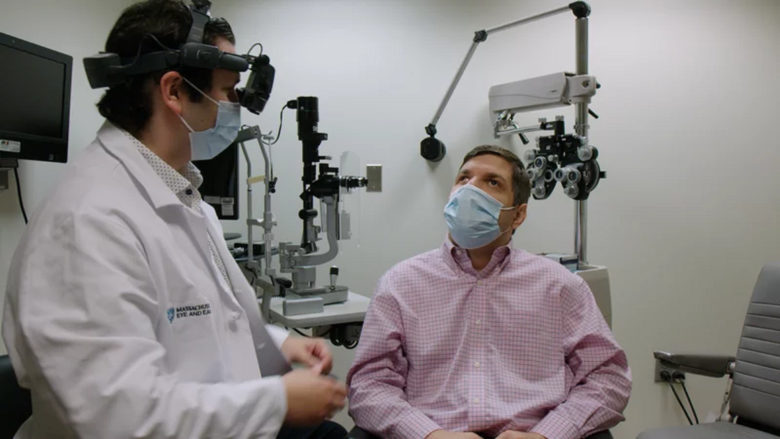
Es ist eines der spannendsten Konzepte der BioTech-Welt: CRISPR, eine Technologie, mit der man gezielt DNA schneiden und verändern kann, quasi eine Schere für Gentechniker. Beispielsweise soll es damit möglich sein, vererbbare Krankheiten auszumerzen. In den USA haben Forscher:innen damit erfolgreich die DNA von Embryonen manipuliert. Nun ist mit dieser Technologie im US-Spezialkrankenhaus Massachusetts Eye and Ear ein bahnbrechendes Experiment erfolgt: Forscher:innen haben Patient:innen mit einer seltenen Augenkrankheit dadurch wieder zu mehr Sehkraft verholfen, schreibt NPR.
„Ich kann Farben leuchtender sehen“
Patientin Carlene Knight leidet wie die anderen Probanden unter der seltenen Erbkrankheit Lebersche kongenitale Amaurose (LCA). Die Krankheit schaltet wichtige Zellen in der Netzhaut aus. Erkrankte leiden schon von Geburt an unter einem fortschreitenden Sehverlust, der sie in der Regel erblinden lässt. Knight konnte durch die Krankheit nur noch sehr schlecht sehen, doch durch das CRISPR-Experiment hat sich ihre Sehkraft massiv erhöht. „Ich habe Farben schon immer geliebt. Schon als Kind konnte ich mich daran erfreuen, wenn ich nur ein wenig sehen konnte. Aber jetzt merke ich, wie viel heller sie in meiner Kindheit waren, weil ich sie jetzt viel leuchtender sehen kann“, sagt sie gegenüber NPR.
CRISPR: Die „Gen-Schere“ fällt laut EuGH unter die strengen Gentechnik-Gesetze
Das Forschungsteam hat für das Experiment, an dem sieben Patient:innen teilgenommen haben, CRISPR auf eine völlig neue Weise verwendet. Sie haben nämlich die Gen-Schere direkt in Zellen injizieren, die sich noch in ihrem Körper befanden. Bei früheren Experimenten haben Wissenschaftler:innen stattdessen immer Zellen aus dem Körper der Probanden entnommen, im Labor bearbeitet und die veränderten Zellen dann die Patient:innen zurückgegeben.
CRISPR direkt in Netzhaut eingeführt
Bei dem Experiment von Massachusetts Eye and Ear war die gewöhnliche Methode jedoch keine Option. Es ist bei der Netzhaut laut dem Team nicht möglich, Zellen zu entfernen und wieder einzusetzen, weswegen die neue Methode zum Einsatz kam. Die Ärzt:innen haben ein harmloses Virus gentechnisch so verändert, dass es den CRISPR-Gen-Editor transportieren konnte. Sie haben Milliarden der veränderten Viren in die Netzhaut der Patient:innen per Infusion eingeführt.
Der CRISPR-Miterfinder in Wien: „Wir sind gar nicht weit weg von Jurassic Park“
Der Eingriff wurde nur an einem Auge durchgeführt, für den Fall, dass etwas schief geht. Sobald das CRISPR-Verfahren in die Zellen der Netzhaut eingedrungen war, sollte das Werkzeug die genetische Mutation, die LCA verursacht, herausschneiden und das Sehvermögen durch Reaktivierung der ruhenden Zellen wiederherstellen.
Signifikante Verbesserung ohne Nebenwirkungen
Nun konnte das Forschungsteam nach mehreren Monaten Beobachtung der Patient:innen erste Ergebnisse liefern. Und siehe da: Die Sehkraft von einigen der Probanden hat sich tatsächlich verbessert. Es hat noch nicht bei allen Patient:innen funktioniert und die Sehkraft wird dadurch nicht völlig wiederhergestellt. Jedoch handle es sich um eine signifikante Verbesserung, die dazu noch ohne nennenswerte Nebenwirkungen ablief. Das sei vor allem vielversprechend, weil es mehrere Krankheiten gibt, bei denen CRISPR nur direkt zum Einsatz kommen kann, darunter Hirnkrankheiten wie Chorea Huntington und Muskelkrankheiten wie Muskeldystrophie.
„Wir sind sehr erfreut über die ersten Anzeichen von Wirksamkeit, denn das bedeutet, dass das Gene Editing funktioniert. Dies ist das erste Mal, dass wir Beweise dafür haben, dass das Gen-Editing in einem Menschen funktioniert und – in diesem Fall – seine Sehfunktion verbessert“, sagt Eric Pierce, Direktor des Ocular Genomics Institute am Massachusetts Eye & Ear. Nun müssen die Forscher:innen überprüfen, ob dieser Ansatz sicher ist. Die derzeitigen Ergebnisse sind jedoch so vielversprechend, dass sie grünes Licht für die nächste Patient:innengruppe erhalten haben.